Tout savoir sur L'eau = h2o
Une molécule d'eau si précieuse à la vie.
L'eau, très présente sur notre Terre et indispensable à la survie de tout être vivant animal ou végétal, n'est pas un liquide banal. Elle a des propriétés physiques fort originales qui résultent de la composition même de sa molécule et de la façon dont ces molécules se lient entre elles. On peut ainsi la trouver sous trois formes : liquide, solide ou gazeuse.
UNE MOLÉCULE SI PRÉCIEUSE
Rappelons que la molécule est le plus petit fragment "possible" d'un corps donné. Elle conserve donc toutes les propriétés physiques et chimiques de celui-ci. Ainsi, en ce qui concerne l'eau, nous atteignons par divisions successives ce "grain" ultime : la molécule d'eau.
Celle-ci a une dimension de l'ordre de 0,0000000001 mètre, soit 0,00000001 cm. La molécule n'est pas une boule. Elle est constituée d'un atome d'oxygène relié à deux petites "boules" qui sont des atomes d'hydrogène. Sa forme est à ce titre souvent comparée à la tête de Mickey. Ces atomes sont liés entre eux par des forces électrostatiques importantes.
LA STRUCTURE DE LA MOLÉCULE D'EAU
Ce n'est que tardivement que la composition de l'eau fut découverte par le physicien anglais Cavendish, à la fin du XVIIIe siècle. Cavendish réussit à démontrer que l'eau était formée d'hydrogène et d'oxygène. Ala même époque, en France, Lavoisier réussissait l'opération inverse : faire de l'eau à partir de ces deux éléments.
Chacun sait aujourd'hui que la molécule d'eau est composée de deux atomes d'hydrogène qui entourent un atome d'oxygène. La formule chimique de l'eau est donc H2o.
Chaque molécule d'eau possède deux pôles chargés électriquement : - Un pôle chargé positivement du côté des atomes d'hydrogène,
- Un pôle chargé négativement du côté des atomes d'oxygène.
Dans une molécule d'eau, les deux atomes d'hydrogène et l'atome d'oxygène complètent leurs couches d'électrons en mettant ceux-ci en commun. Chaque atome d'hydrogène, avec un électron seulement en orbite autour de son noyau, a besoin d'un électron supplémentaire pour atteindre un état stable. L'atome d'oxygène avec ses six électrons sur la couche externe, en a besoin de deux autres pour compléter celle-ci. Lorsque ces trois atomes instables mettent en commun leurs électrons, ils forment une molécule d'eau stable.
Ce n'est pas dévoiler un secret aujourd'hui que de dire que la molécule d'eau est composée de deux atomes d'hydrogène qui entourent un atome d'oxygène. La formule chimique de l'eau est donc H2O. 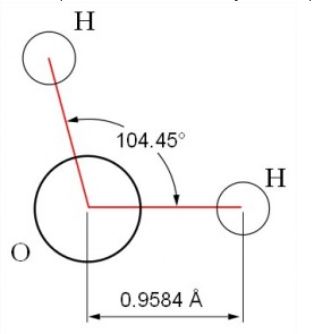 Dans une molécule d'eau, les deux atomes d'hydrogène et l'atome d'oxygène complètent leurs couches d'électrons en mettant ceux-ci en commun. Chaque atome d'hydrogène, avec un électron seulement en orbite autour de son noyau, a besoin d'un électron supplémentaire pour atteindre un état stable. L'atome d'oxygène avec ses six électrons sur la couche externe, en a besoin de deux autres pour compléter celle-ci. Lorsque ces trois atomes instables mettent en commun leurs électrons, ils forment une molécule d'eau stable.
|
LES TROIS ÉTATS DE L'EAULES TROIS ÉTATS DE L'EAU
L'eau, sous l'action conjuguée de la chaleur et de la pression atmosphérique, change d'état, passant de celui de vapeur à l'état solide ou liquide.
- L'état de vapeur (état gazeux)
Le phénomème d'évaporation de l'eau, c'est à dire le passage de l'eau de l'état liquide à l'état de vapeur est très important. L'eau, en se transformant en vapeur, passe à l'état gazeux qui est celui du désordre maximal des molécules, ces dernières sont tellement agitées que les forces d'attraction terrestre s'exercent de façon beaucoup moins forte.
Ce phénomène se produit à partir des plans d'eau, des sols humides, mais aussi dans ce qu'on appelle l'évapotranspiration, par l'intermédiaire de l'extraction racinaire de l'eau du sol et ensuite par la transpiration de cette eau par les feuilles des plantes. L'eau évaporée va transiter dans l'atmosphère sous forme de vapeur invisible où elle reste pendant huit jours en moyenne. Puis l'eau va former des nuages qui vont retomber en pluie sur les continents et les océans. Le cycle de l'eau dans l'atmosphère sous forme de vapeur est assez court mais cependant vital car c'est la vapeur d'eau qui est à l'origine des 520 km3 de précipitations que ce soit sous la forme de pluie, de neige ou de grêle, qui alimentent les réserves d'eau douce.
Par rapport à la masse totale de l'hydrosphère, la vapeur d'eau ne représente qu'une toute petite quantité puisqu'elle est égale à 0,001 % de la totalité de l'eau.
C'est la forme de l'eau la plus répandue sur Terre. Il y a d'une part l'eau douce qui représente seulement 2,8 % de l'eau totale du globe. Dans ce faible pourcentage, les glaces polaires représentent 2,15 %, les eaux souterraines 0,63 %, les eaux de surface (lacs, fleuves et rivières) seulement 0,019 %. Reste 0,001 % pour l'atmosphère. L'eau douce contenue dans les glaciers est cependant très difficilement accessible à l'homme.
Le reste, c'est à dire l'eau salée, est contenu dans les mers et des océans. Ces derniers représentent 90 % de l'hydrosphère et couvrent plus de 71 % de la surface terrestre.
Une partie des 2,8 % d'eau douce, soit un volume de 30 100 000 km3, est stockée sous forme de glaciers ou sous forme de neige, soit 2,15 % de l'eau sur terre.
En fonction de l'altitude et de la température, les précipitations se font sous forme de neige ou de pluie. La neige est seulement un stockage temporaire appelé à disparaître lors du redoux. Lorsque la température remonte, soit la neige retourne directement vers l'atmosphère par évaporation, c'est de la sublimation, soit la fonte lente du manteau neigeux va permettre à l'eau de s'infiltrer dans le sol ou de ruisseler vers les rivières.
Les glaciers représentent actuellement 10 % des terres émergées, ils sont surtout présents aux pôles. Les calottes glaciaires des pôles Nord et Sud sont les plus grands réservoirs d'eau douce de la planète. Les glaciers sont alimentés en surface par la neige. Ils ne sont pas immobiles mais s'écoulent lentement, emportés par leur propre poids, vers l'aval. Suivant le type de glaciers, leur vitesse de déplacement peut atteindre un mètre par jour ou par an. La masse des glaciers est très importante et, s'ils devaient fondre, le niveau des mers remonterait de près de deuxcent mètres.
L'eau, sous l'action conjuguée de la chaleur et de la pression atmosphérique, change d'état. On la trouve naturellement dans 3 états : - L'état de vapeur (état gazeux) - L'état liquide - L'état solide 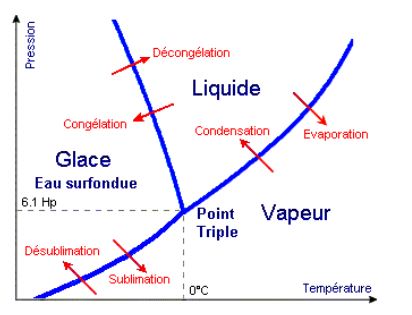 EAU ET HYDROGENE
LA LIAISON HYDROGÈNE
Chaque goutte d'eau contient plusieurs milliards de molécules d'eau, reliées les unes aux autres par leurs pôles, chargés électriquement : un pôle chargé négativement (l'atome d'oxygène) et un pôle chargé positivement (les atomes d'hydrogène).
En présence les unes des autres, les molécules vont se comporter comme de petits aimants : leurs pôles électriques positifs et négatifs s'attirent réciproquement et les molécules se rapprochent afin que chaque atome d'hydrogène (positif) de l'une se place près de l'oxygène (négatif) d'une voisine.
Les molécules d'eau sont alors liées par ce que l'on appelle une liaison hydrogène, cette liaison étant assurée par les atomes d'hydrogène. Ainsi, l'eau n'est pas un liquide ordinaire : au sein d'une même masse d'eau, la plupart des molécules sont liées entre elles en une sorte de réseau sans cesse changeant et modulable d'une fraction de seconde à l'autre. En effet, si l'union à l'intérieur même d'une molécule, est très stable, il n'est est pas de même en ce qui concerne les liens entre les molécules. Ces dernières sont à la fois très proches et très libres, elles se lient entre elles et se défont tout aussi rapidement, elles "roulent" les unes sur les autres, changeant sans cesse leur ordonnancement. Cette liaison hydrogène est donc plus faible que celle qui soude entre eux les trois atomes de la molécule, mais cependant suffisamment forte pour expliquer les propriétés exceptionnelles de l'eau. Dans l'eau, les molécules H2o ont une telle attirance électrique les unes pour les autres qu'il arrive qu'un atome d'hydrogène de l'une soit capté par l'atome d'oxygène de l'autre. Cet échange transforme les deux molécules H2o de départ en H3o et OH ; le nombre d'atomes et de charges électriques + et – n'est plus le même de chaque côté : d'un côté on trouve OH- et de l'autre H3o+. Ces molécules modifiées s'appellent des ions et leurs propriétés s'annulent : l'eau est électriquement neutre.
L'EAU DANS L'UNIVERS
L'eau peut se former spontanément à partir de deux atomes d'hydrogène et d'un atome d'oxygène, mais seulement sous certaines conditions : - Des quantités suffisantes d'oxygène et d'hydrogène,
- Une température pas trop élevée (pas plus de 2 000 à 3000°C)
- Un rayonnement ultraviolet pas trop important.
Or, ces conditions sont difficiles à réunir. En particulier, l'univers comporte 90 % d'hydrogène contre "seulement" 0,1 % d'oxygène.
En l'état actuel de nos connaissances, la Terre est la seule planète du système solaire comprenant de l'eau liquide. Nous vivons donc bien sur la planète de l'eau... qui est aussi la planète de la vie.
DE L'UNIVERS AU MONDE DE L'EAU
DE L'UNIVERS AU MONDE DE L'EAU
Pour la quasi-totalité de la communauté scientifique, l'univers est né il y a quelque 15 milliards d'années, d'une extraordinaire explosion. Après ce Big Bang, un formidable chaos provoque nuages de gaz et de poussières. Et, à partir de l'un deux, la Terre se forme... Cette "apparition" date de 4,6 milliards d'années... C'est alors une grosse boule chaude d'aspect lunaire...
Une météorite frappe ensuite de plein fouet la planète et crée en sa surface l'océan primitif. Cette première forme d'eau donne naissance,il y a 3,5 milliards d'années, aux premières formes de vie. Un scénario qui confère donc déjà à la Terre un caractère unique dans le système solaire. L'eau enfouie à l'intérieur du globe jaillit des volcans sous forme de vapeur. Puis la Terre se refroidit. La vapeur, en se condensant, provoque des pluies diluviennes qui ruissellent - se chargeant au passage de sels minéraux. Cette eau salée forme des océans. Pendant ce temps-là, au sein de l'atmosphère, les pluies et la vapeur constituent la première réserve d'eau douce. Celle-là même que nous puisons encore aujourd'hui...
L'EAU SUR LA PLANÈTE
L'eau recouvre 72 % des 509 millions de km2 de la surface du globe. On estime son volume à environ 1400 000 000 km3 soit 1 400 000 000 000 000 000 000 litres (1 km3 = 1 000 000 000 m3 et 1 m3 = 1000 litres). Ce qui représente un cube de plus de 1000 km de côté. Ce volume d'eau est stable.
L'eau de la planète bleue est à 97,2 % salée. Cette eau salée se retrouve dans les océans, les mers intérieures, mais aussi dans certaines nappes souterraines. L'eau douce, elle, représente donc 2,8 % de l'eau totale du globe. Dans ce faible pourcentage, les glaces polaires représentent 2,15%, les eaux souterraines 0,63 %, les eaux de surface (lacs, fleuves et rivières) seulement 0,019 %. Reste 0,001 % pour l'atmosphère. |
Plus d'infos
Sources : OMS, DGS Cliquez ici pour modifier le texte. Nos matériels d'économie d'eau permettent de réduire de 40 à 60 % le débit de l'eau, sans altérer le confort. Nos actions portent principalement sur les points d'eau suivants :- robinets : débit standart 12 L/min, mousseur économique 5 L/min, soit - 60% - douches fixes ou douchettes : débit standart 14 L/min,douchette économique 6 L/min, soit - 60% - réservoirs de WC : débit standart 10 L, WC économique 6 L, soit - 40% Si vous souhaitez des informations sur le matériel d'économie d'eau, cliquer ci-dessous: eau économisée sur la douche
eau économisée sur les robinets
eau économisée sur les WC |